Содержание
1. Среднее значение мольной теплоёмкости метана при постоянном объёме выражается уравнением 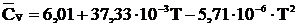 . Найдите значение истинной мольной изобарной теплоёмкости метана при 600 К.
. Найдите значение истинной мольной изобарной теплоёмкости метана при 600 К.
Решение
2. Рассчитайте температуру кипения водного раствора, содержащего 0,02 моля растворенного вещества (неэлектролита) в 100 г воды.
Решение
3. Пользуясь справочными данными, вычислите тепловой эффект, стандартное химическое сродство и константу равновесия реакции Fe + H20 Fe3O4 + 4H2 при температуре Т = 900 К. По полученным значениям определите направление и глубину протекания (качественно) реакции при заданной температуре.
Таблица 1. Значения Мn для вычисления термодинамических величин по методу Темкина и Шварцмана
|
Т, К |
Мо |
М1 10-3 |
М2 10-6 |
М-2 105 |
|
900 |
0,436 |
0,201 |
0,100 |
0,252 |
Таблица 2. Термодинамические константы веществ в стандартных условиях
|
Вещество |
кДж/моль |
кДж/моль |
Дж/моль∙К |
Теплоёмкость, Дж/моль∙К. Коэффициенты уравнения |
Температурный интервал, К |
|||
|
а |
||||||||
|
(кр.α) |
0 |
0 |
27,15 |
17,24 |
24,77 |
|
- |
298 – 1000 |
|
(г) |
-241,82 |
-228,61 |
188,72 |
30,00 |
10,71 |
|
0,33 |
298 – 2500 |
|
(кр.) |
-264,85 |
-244,30 |
60,75 |
50,80 |
8,61 |
|
-3,31 |
298 – 1650 |
|
(г) |
0 |
0 |
130,52 |
27,28 |
3,26 |
|
0,50 |
298 – 3000 |
Вы можете убедиться в качестве данной работы:
![fizicheskaya-himiya-3-zadachi--reshenie.[1]](/writable/files/rfm_source/21february2020/fizicheskaya-himiya-3-zadachi--reshenie.%5B1%5D.png)









